 | |
| Data klinis | |
|---|---|
| Nama dagang | Visudyne |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a607060 |
| License data | |
| Rute pemberian | Intravena |
| Kode ATC | |
| Status hukum | |
| Status hukum |
|
| Pengenal | |
| |
| Nomor CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| Data sifat kimia dan fisik | |
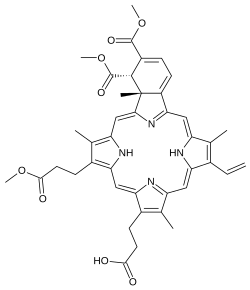
| Rumus | C41H42N4O8 |
| Massa molar | 718,81 g·mol−1 |
| Model 3D (JSmol) | |
| |
| |
| | |
Verteporfin merupakan turunan benzoporfirin, yang digunakan sebagai fotosensitizer untuk terapi fotodinamik, untuk menghilangkan pembuluh darah abnormal di mata yang terkait dengan kondisi seperti degenerasi makula bentuk basah. Verteporfin terakumulasi dalam pembuluh darah abnormal ini, dan ketika dirangsang oleh cahaya merah nontermal dengan panjang gelombang 689 nm[1] dengan adanya oksigen, menghasilkan oksigen singlet berumur pendek yang sangat reaktif dan radikal bebas oksigen reaktif lainnya, yang mengakibatkan kerusakan lokal pada endotelium dan penyumbatan pembuluh darah.[2][3] Verteporfin juga digunakan di luar label untuk pengobatan retinopati serosa sentral.[4]
Pemberian
suntingVerteporfin biasanya disuntikkan secara intravena ke dalam vena lengan terbesar. Disuntikkan dengan dosis 6 mg/m2 dan diaktifkan dengan cahaya.[5] Biasanya diberikan 15 menit sebelum perawatan laser.[2] Dosis ini dapat diulang 4 kali per tahun.[5]
Kontraindikasi
suntingBagian ini memerlukan pengembangan. Anda dapat membantu dengan mengembangkannya. (Juli 2025) |
- Porfiria: Pasien dengan porfiria tidak boleh menerima verteporfin karena risiko memperburuk kondisi ini.[2][6]
- Hipersensitivitas: Pasien dengan hipersensitivitas yang diketahui terhadap verteprofin atau bahan apa pun yang digunakan dalam formulasinya harus menghindari penggunaan obat ini.[7]
Efek samping
suntingEfek samping yang paling umum adalah penglihatan kabur, sakit kepala, dan efek lokal di tempat suntikan. Selain itu juga dapat terjadi fotosensitivitas, sehingga sangat disarankan untuk menghindari paparan sinar matahari dan pencahayaan tanpa pelindung hingga 48 jam setelah pemberian verteporfin.[2]
Anjing dan tikus telah diobati dengan dosis harian inaktif 32–70 kali lebih tinggi daripada dosis yang disarankan untuk manusia.[5] 4 minggu pengobatan mengakibatkan hemolisis ekstravaskular ringan dan hematopoiesis pada hewan.[5]
Sitotoksisitas yang diaktifkan cahaya
suntingBila digunakan sendiri, dosis klinis yang direkomendasikan untuk verteporfin tidak bersifat sitotoksik terhadap jaringan manusia. Meskipun diaktifkan oleh cahaya dengan adanya oksigen, ia dapat membentuk agen sitotoksik di dalam jaringan. Agen terbentuk ketika porfirin menyerap cukup cahaya untuk menghasilkan oksigen singlet yang reaktif tetapi berumur pendek. Oksigen singlet yang singkat dapat merusak struktur biologis secara mikro, yang menyebabkan oklusi vaskular lokal.[8]
Interaksi
suntingVerteporfin diketahui berinteraksi dengan obat herbal yang bwrasal dari Tanacetum parthenium, yang tampaknya bertindak sebagai antagonis verteporfin karena alasan yang belum diketahui. Mengonsumsi kedua zat tersebut secara bersamaan tidak disarankan.[9]
Verteporfin tampaknya tidak dimetabolisme oleh enzim sitokrom P450, sehingga tidak memengaruhi metabolisme sitokrom P450 obat lain.[10]
Kekurangan
suntingPada bulan Mei 2020, kapasitas produksi yang rendah menyebabkan gangguan. Hal ini memengaruhi penggunaan verteporfin di kalangan penyedia layanan kesehatan dan pasien di Eropa. EMA memperkirakan produksi normal akan kembali pada kuartal pertama tahun 2022.[11]
Penggunaan di luar label
suntingVerteporfin dapat digunakan di luar label untuk mengobati retinopati serosa sentral[4][11] dan diterapkan secara eksperimental untuk mengurangi jaringan parut pada transplantasi rambut.[12]
Referensi
sunting- ^ "Visudyne package insert" (PDF).
- ^ a b c d Verteporfin monograph
- ^ Scott LJ, Goa KL (February 2000). "Verteporfin". Drugs & Aging. 16 (2): 139–46, discussion 147–8. doi:10.2165/00002512-200016020-00005. PMID 10755329. S2CID 260491296.
- ^ a b Karim SP, Adelman RA (2013). "Profile of verteporfin and its potential for the treatment of central serous chorioretinopathy". Clinical Ophthalmology. 7: 1867–75. doi:10.2147/OPTH.S32177. PMC 3788817. PMID 24092965.
- ^ a b c d Mohede, Daan C.J. (28 September 2018), "Verteporfin as a Medical Treatment in Peyronie's Disease", Sex Med (dalam bahasa English), 6 (4): 302–308, doi:10.1016/j.esxm.2018.08.002, PMC 6302152, PMID 30274909 Pemeliharaan CS1: Bahasa yang tidak diketahui (link)
- ^ "Verteporfin Injection: MedlinePlus Drug Information". medlineplus.gov (dalam bahasa Inggris). Diakses tanggal 2025-05-28.
- ^ "Verteporfin Monograph for Professionals". Drugs.com (dalam bahasa Inggris). Diakses tanggal 2025-05-28.
- ^ "SUMMARY OF PRODUCT CHARACTERISTICS" (PDF). ema.europa.eu. 13 December 2023. Diarsipkan dari asli (PDF) tanggal 2023-12-13. Diakses tanggal 13 December 2023.
By itself, the clinically recommended dose of verteporfin is not cytotoxic. It produces cytotoxic agents only when activated by light in the presence of oxygen. When energy absorbed by the porphyrin is transferred to oxygen, highly reactive short-lived singlet oxygen is generated. Singlet oxygen causes damage to biological stmctures within the diffusion range, leading to local vascular occlusion, cell damage and, under certain conditions, cell death.
- ^ "Feverfew and Verteporfin Interactions". Drugs.com. Diakses tanggal 14 April 2015.
- ^ "Visudyne (verteporfin for injection) prescribing information" (PDF). FDA. Diarsipkan dari asli (PDF) tanggal February 28, 2017. Diakses tanggal 12 April 2021.
- ^ a b EMA (5 November 2021). "Shortage of Visudyne (verteporfin)" (PDF). ema.europa.eu. Diakses tanggal 1 February 2022.
- ^ "American Hair Loss Society".
Pranala luar
sunting- "Visudyne". Novartis.