Anoda adalah elektrode, bisa berupa logam maupun penghantar listrik lain, pada sel elektrokimia yang terpolarisasi jika arus listrik mengalir ke dalamnya. Arus listrik (bermuatan positif) mengalir berlawanan dengan arah pergerakan elektron.[1] Pada proses elektrokimia, baik sel galvanik (baterai) maupun sel elektrolisis, anode mengalami oksidasi.[2]
Perlu diperhatikan bahwa tidak selalu anion (ion yang bermuatan negatif) bergerak menuju anode, ataupun tidak selalu kation (ion bermuatan positif) akan bergerak menjauhi anode. Pergerakan anion maupun kation menuju atau menjauh dari anode tergantung dari jenis sel elektrokimianya.
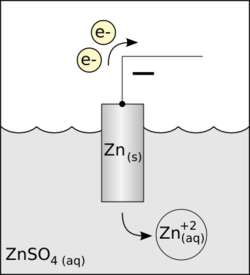
- Pada sel galvanik atau pembangkit listrik (baterai), anode adalah kutub negatif. Elektrode akan melepaskan elektron menuju ke sirkuit dan karenanya arus listrik mengalir ke dalam elektrode ini dan menjadikannya anode dan berkutub negatif. Dalam sel galvanik, reaksi oksidasi terjadi secara spontan. Karena terus menerus melepaskan elektron anode cenderung menjadi bermuatan positif dan menarik anion dari larutan (elektrolit) serta menjauhkan kation. Dalam contoh gambar diagram anode seng (Zn) di kanan, anion adalah SO4−2, kation adalah Zn2+ dan ZnSO4 elektrolit.
- Pada sel elektrolisis, anode adalah elektrode positif. Arus listrik dari kutub positif sumber tegangan listrik luar (GGL) dialirkan ke elektrode sehingga memaksa elektrode tereduksi dan melepaskan elektron.
Lihat pula
sunting- Katode
- Anion
- Kation
- Larutan elektrolit
- Redoks (oksidasi-reduksi)
- Sel galvanik
- Sel elektrolisis
- Baterai
- Anodisasi (proses perlindungan permukaan aluminium)
- Proteksi katodik
Pranala luar
suntingReferensi
sunting- ^ Ph. D., Biomedical Sciences; B. A., Physics and Mathematics; Facebook, Facebook; Twitter, Twitter. "Anode vs. Cathode: What's the Difference?". ThoughtCo (dalam bahasa Inggris). Diakses tanggal 2020-10-30.
- ^ "Cathode And Anode - Definition, Examples and Key Differences". BYJUS (dalam bahasa American English). Diakses tanggal 2020-10-30.