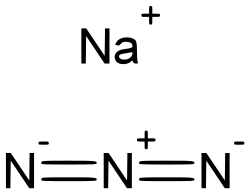
| |

| |
| Nama | |
|---|---|
| Nama lain
Natrium trinitrida
Smite Azium | |
| Penanda | |
Model 3D (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| Nomor UN | 1687 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| NaN3 | |
| Massa molar | 65.0099 g/mol |
| Penampilan | padatan tak berwarna hingga putih |
| Bau | tak berbau |
| Densitas | 1.846 g/cm3 (20 °C) |
| Titik lebur | 275 °C penguraian keras |
| 38.9 g/100 mL (0 °C) 40.8 g/100 mL (20 °C) 55.3 g/100 mL (100 °C) | |
| Kelarutan | sangat larut dalam amonia agak larut dalam benzena tidak larut dalam eter, aseton, heksana, kloroform |
| Kelarutan dalam metanol | 2.48 g/100 mL (25 °C) |
| Kelarutan dalam ethanol | 0.22 g/100 mL (0 °C) |
| Keasaman (pKa) | 4.8 |
| Struktur | |
| Heksagonal, hR12[1] | |
| R-3m, No. 166 | |
| Termokimia | |
| Kapasitas kalor (C) | 76.6 J/mol K |
| Entropi molar standar (S |
70.5 J/mol K |
| Entalpi pembentukan standar (ΔfH |
21.3 kJ/mol |
| Energi bebas Gibbs (ΔfG) | 99.4 kJ/mol |
| Bahaya | |
| Lembar data keselamatan | External MSDS |
Klasifikasi UE (DSD) (usang)
|
Sangat beracun (T+) Sangat berbahaya bagi lingkungan (N) |
| Frasa-R | R28, R32, R50/53 |
| Frasa-S | (S1/2), S28, S45, S60, S61 |
| Titik nyala | 300 °C (572 °F; 573 K) |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
27 mg/kg (oral, tikus)[1] |
| Batas imbas kesehatan AS (NIOSH): | |
PEL (yang diperbolehkan)
|
none[2] |
REL (yang direkomendasikan)
|
C 0.1 ppm (sebagai HN3) [kulit] C 0.3 mg/m3 (sebagai NaN3) [kulit][2] |
IDLH (langsung berbahaya)
|
N.D.[2] |
| Senyawa terkait | |
Anion lain
|
Natrium sianida |
Kation lainnya
|
Kalium azida Amonium azida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Natrium azida adalah suatu senyawa anorganik dengan kimia NaN3. Garam tak berwarna ini adalah komponen pembentuk gas dalam banyak sistem kantung udara mobil. Senyawa ini digunakan untuk pembuatan senyawa azida lainnya. Senyawa ini adalah zat ionik, sangat mudah larut air, dan sangat beracun.
Struktur
suntingNatrium azida adalah padatan ionik. Dua bentuk kristalnya diketahui, rombohedral dan heksagonal.[1][4] Keduanya mengadopsi struktur berlapis. Anion azida sangat mirip pada masing-masing bentuk, dengan sentrosimetris dengan jarak N–N sebesar 1.18 Å. Ion Na+ memiliki geometri oktahedral. Setiap azida terhubung dengan enam pusat Na+, dengan tiga ikatan Na-N di setiap ujung pusat nitrogen.[5]
Preparasi
suntingMetode sintesis yang umum adalah "proses Wislicenus" yang berlangsung dalam dua tahapan dari amonia. Pada tahap pertama, amonia diubah menjadi natrium amida:
- 2 Na + 2 NH3 → 2 NaNH2 + H2
Natrium amida kemudian digabungkan dengan dinitrogen oksida:
- 2 NaNH2 + N2O → NaN3 + NaOH + NH3
Reaksi ini adalah dasar dari jalur industri, yang menghasilkan sekitar 250 ton/tahun pada tahun 2004, dengan produksi meningkat karena mempopulerkan kantung udara[6]
Reaksi
suntingPerlakuan natrium azida dengan asam kuat memberi asam hidrazoat, yang juga sangat toksik:
- H+ + N−3 → HN3
Larutan berair mengandung sejumlah kecil hidrogen azida, pembentukan yang digambarkan oleh kesetimbangan berikut:
- N−3 + H2O ⇌ HN3 + OH− (K = 10−4.6)
Natrium azida dapat dihancurkan dengan perlakuan dengan larutan asam nitrit:[7]
- 2 NaN3 + 2 HNO2 → 3 N2 + 2 NO + 2 NaOH
Aplikasi
suntingKantung udara mobil dan pesawat lepas landas
suntingFormulasi kantung udara yang lebih tua mengandung campuran oksidasi dan natrium azida dan zat lainnya termasuk ignitor dan akselerator. Pengendali elektronik meledakkan campuran ini selama terjadi kecelakaan mobil:
- 2 NaN3 → 2Na + 3 N2
Reaksi yang sama terjadi saat memanaskan garam sampai kira-kira 300 °C. Natrium yang terbentuk merupakan bahaya potensial saja dan, di kantung udara mobil, diubah oleh reaksi dengan bahan lain, seperti kalium nitrat dan silika. Dalam kasus terakhir, natrium silikat yang tidak berbahaya dihasilkan.[8] Natrium azida juga digunakan dalam pelarian pesawat terbang. Kantung udara generasi baru mengandung nitroguanidin atau bahan peledak yang kurang sensitif.
Sintesis organik dan anorganik
suntingKarena bahaya ledakannya, natrium azida hanya memiliki nilai terbatas dalam kimia organik skala industri. Di laboratorium, digunakan sintesis organik untuk memperkenalkan gugus fungsional azida dengan perpindahan halida. Gugus fungsional azida kemudian dapat dikonversi menjadi amina dengan reduksi dengan SnCl2 dalam etanol atau litium aluminium hidrida atau fosfin tersier, seperti trifenilfosfin dalam reaksi Staudinger, dengan nikel Raney atau dengan hidrogen sulfida dalam piridin.
Natrium azida adalah prekursor serbaguna untuk senyawa azida anorganik lainnya, misalnya, timbal azida dan perak azida, yang digunakan dalam bahan peledak.
Penggunaan biokimia dan biomedis
suntingNatrium azida adalah pereaksi penjejak yang berguna dan pengawet.
Di rumah sakit dan laboratorium, senyawa ini adalah biosida; senyawa ini terutama penting dalam pereaksi curah dan larutan stok yang dapat mendukung pertumbuhan bakteri dimana natrium azida berperan sebagai bakteriostatik dengan menghambat sitokrom oksidase dalam bakteri gram negatif; gram positif (streptococcus, pneumococci, lactobacilli) secara intrinsik resisten.[9]
Penggunaan pertanian
suntingSenyawa ini digunakan dalam pertanian untuk pengendalian hama patogen yang ditanggung tanah seperti Meloidogyne incognita atau Helicotylenchus dihystera.[10]
Senyawa ini juga digunakan sebagai mutagen untuk pemilihan tanaman tanaman seperti padi,[11] barley[12] atau oat.[13]
Keamanan
suntingNatrium azida telah menyebabkan kematian selama beberapa dekade.[14] Senyawa ini adalah racun yang parah. Mungkin berakibat fatal jika kena kulit atau jika tertelan.[15] Bahkan jumlah menit pun bisa menimbulkan gejala. Toksisitas senyawa ini sebanding dengan sianida alkali yang dapat larut dan dosis mematikan untuk manusia dewasa sekitar 0,7 gram.[16] Tidak ada toksisitas yang dilaporkan dari kantung udara bekas.[17]
Azida menghambat sitokrom oksidase dengan mengikat secara ireversibel ke kofaktor heme dalam proses yang serupa dengan aksi karbon monoksida. Natrium azida terutama mempengaruhi organ yang mengalami tingkat respirasi tinggi, seperti jantung dan otak.
Senyawa ini menghasilkan gejala ekstrapiramidal dengan nekrosis korteks otak besar, otak kecil, dan ganglia basal. Toksisitas juga bisa meliputi hipotensi,[18] Kebutaan dan nekrosis hati. Natrium azida meningkatkan kadar GMP siklik di otak dan hati dengan aktivasi guanilat siklase.[19]
Referensi
sunting- ^ a b c Stevens E. D.; Hope H. (1977). "A Study of the Electron-Density Distribution in Sodium Azide, NaN3". Acta Crystallographica A. 33 (5): 723–729. doi:10.1107/S0567739477001855.
- ^ a b c "NIOSH Pocket Guide to Chemical Hazards #0560". National Institute for Occupational Safety and Health (NIOSH).
- ^ "Material Safety Data Sheet" (PDF). Sciencelab.com. November 6, 2008. Diarsipkan dari asli (PDF) tanggal 2016-03-04. Diakses tanggal October 2015. ;
- ^ Wells, A. F. (1984), Structural Inorganic Chemistry (Edisi 5th), Oxford: Clarendon Press, ISBN 0-19-855370-6
- ^ Pringle, G. E.; Noakes, D. E. (1968-02-15). "The crystal structures of lithium, sodium and strontium azides". Acta Crystallographica Section B. 24 (2): 262–269. doi:10.1107/s0567740868002062.
- ^ Jobelius, Horst H.; Scharff, Hans-Dieter (2000-01-01). Hydrazoic Acid and Azides. Wiley-VCH Verlag GmbH & Co. KGaA. doi:10.1002/14356007.a13_193. ISBN 9783527306732.
- ^ Committee on Prudent Practices for Handling, Storage, and Disposal of Chemicals in Laboratories, Board on Chemical Sciences and Technology, Commission on Physical Sciences, Mathematics, and Applications, National Research Council (1995). "Disposal of Waste". Prudent Practices in the Laboratory: Handling and Disposal of Chemicals. Washington, DC: National Academy Press. hlm. 165. ISBN 0-309-05229-7. Pemeliharaan CS1: Banyak nama: authors list (link)
- ^ Betterton, E. A. (2003). "Environmental Fate of Sodium Azide Derived from Automobile Airbags". Critical Reviews in Environmental Science and Technology. 33 (4): 423–458. doi:10.1080/10643380390245002.
- ^ Lichstein, H. C.; Soule, M. H. (1943). "Studies of the Effect of Sodium Azide on Microbic Growth and Respiration: I. The Action of Sodium Azide on Microbic Growth". Journal of Bacteriology. 47 (3): 221–230. PMC 373901. PMID 16560767.
- ^ Applications of sodium azide for control of soilborne pathogens in potatoes. Rodriguez-Kabana, R., Backman, P. A. and King, P.S., Plant Disease Reporter, 1975, Vol. 59, No. 6, pp. 528-532 (link)
- ^ Awan, M. Afsar; Konzak, C. F.; Rutger, J. N.; Nilan, R. A. (2000-01-01). "Mutagenic Effects of Sodium Azide in Rice1". Crop Science. 20 (5): 663–668. doi:10.2135/cropsci1980.0011183x002000050030x.
- ^ Cheng, Xiongying; Gao, Mingwei. "Biological and genetic effects of combined treatments of sodium azide, gamma rays and EMS in barley". Environmental and Experimental Botany. 28 (4): 281–288. doi:10.1016/0098-8472(88)90051-2.
- ^ Rines, H. W. (1985-02-01). "Sodium azide mutagenesis in diploid and hexaploid oats and comparison with ethyl methanesulfonate treatments". Environmental and Experimental Botany. 25 (1): 7–16. doi:10.1016/0098-8472(85)90043-7.
- ^ Chang, Soju; Lamm, Steven H. (2003-05-01). "Human Health Effects of Sodium Azide Exposure: A Literature Review and Analysis". International Journal of Toxicology. 22 (3): 175–186. doi:10.1080/10915810305109. ISSN 1091-5818. PMID 12851150.
- ^ Richardson, S. G.; Giles, C.; Swan, C. H. (1975-05-01). "Two cases of sodium azide poisoning by accidental ingestion of Isoton". Journal of Clinical Pathology. 28 (5): 350–351. doi:10.1136/jcp.28.5.350. ISSN 1472-4146. PMC 475710. PMID 1150884.
- ^ "MSDS: sodium azide". Mallinckrodt Baker. 2008-11-21. MSDS S2906.
- ^ Olson, Kent; Anderson, Ilene B. (18 September 2006). Poisoning & Drug Overdose, 5th Edition. McGraw-Hill Companies,Incorporated. hlm. 123–. ISBN 978-0-07-144333-3.
- ^ "Kidney International - Abstract of article: Epidemic hypotension in a dialysis center caused by sodium azide". Kidney Int. 37 (1): 110–115. 1990-01-01. doi:10.1038/ki.1990.15. ISSN 0085-2538.
- ^ Kimura, Hiroshi; Mittal, Chandra K.; Murad, Ferid (1975-10-23). "Increases in cyclic GMP levels in brain and liver with sodium azide an activator of guanylate cyclase". Nature. 257 (5528): 700–702. doi:10.1038/257700a0.