
| |||
| |||
| |||
 Sel satuan natriun nitrit dalam kondisi standar.
| |||
| Penanda | |||
|---|---|---|---|
Model 3D (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
| UNII | |||
| Nomor UN | 1500 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| NaNO2 | |||
| Massa molar | 68.9953 g/mol | ||
| Penampilan | padatan putih atau agak kekuningan | ||
| Densitas | 2.168 g/cm3 | ||
| Titik lebur | 271 °C (terurai pada 320 °C) | ||
| 71.4 g/100 mL (0 °C) 84.8 g/100 mL (25 °C) 160 g/100 mL (100 °C) | |||
| Kelarutan | larut dalam metanol (4.4 g/100 mL) etanol agak larut dalam dietil eter (0.3 g/100 mL) sangat larut dalam amonia | ||
| Keasaman (pKa) | ~9 | ||
| −14.5·10−6 cm3/mol | |||
| Indeks bias (nD) | 1.65 | ||
| Struktur[1] | |||
| ortorombik | |||
| Im2m | |||
a = 3.5653(8) Å, b = 5.5728(7) Å, c = 5.3846(13) Å
| |||
Satuan formula (Z)
|
2 | ||
| Termokimia | |||
| Entropi molar standar (S |
106 J/mol K | ||
| Entalpi pembentukan standar (ΔfH |
−359 kJ/mol[2] | ||
| Energi bebas Gibbs (ΔfG) | −295 kJ/mol | ||
| Farmakologi | |||
| Kode ATC | V03 | ||
| Bahaya | |||
| Lembar data keselamatan | External MSDS | ||
Klasifikasi UE (DSD) (usang)
|
|||
| Frasa-R | R8, R25, R50 | ||
| Frasa-S | (S1/2), S45, S61 | ||
| 489 °C (912 °F; 762 K) | |||
| Dosis atau konsentrasi letal (LD, LC): | |||
LD50 (dosis median)
|
180 mg/kg (tikus, oral) | ||
| Senyawa terkait | |||
Anion lain
|
Natrium nitrat | ||
Kation lainnya
|
Kalium nitrit Amonium nitrit Litium nitrit | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
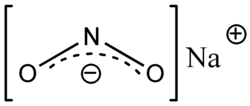
Natrium nitrit adalah suatu senyawa anorganik dengan rumus kimia NaNO2. Senyawa ini adalah bubuk kristalin putih hingga agak kekuningan yang sangat larut dalam air dan higroskopis. Senyawa ini adalah prekursor berguna bagi berbagai senyawa organik, seperti obat-obatan, pewarna, dan pestisida, tetapi mungkin paling dikenal sebagai aditif dalam daging untuk mencegah botulisme.
Senyawa ini termasuk dalam Daftar Obat Esensial Organisasi Kesehatan Dunia, obat terpenting yang dibutuhkan dalam sistem kesehatan dasar.[3]
Produksi
suntingGaram ini disiapkan dengan mereaksikan natrium hidroksida dengan campuran nitrogen dioksida dan nitrogen monoksida:
- 2 NaOH + NO2 + NO → 2 NaNO2 + H2O
Reaksi di atas sangat peka terhadap keberadaan oksigen, yang dapat menghasilkan natrium nitrat dalam jumlah yang beragam.
Di masa lalu, natrium nitrit dibuat dengan mereduksi natrium nitrat dengan berbagai logam.[4][5]
Reaksi kimia
suntingDi laboratorium, natrium nitrit dapat digunakan untuk menghilangkan kelebihan natrium azida.[6][7]
- 2 NaN3 + 2 NaNO2 + 2 H+ → 3 N2 + 2 NO + 2 Na+ + 2 H2O
Di atas 330 °C natrium nitrit terurai (di udara) menjadi natrium oksida, nitrogen monoksida dan nitrogen dioksida.[8]
- 2 NaNO2 → Na2O + NO + NO2
Natrium nitrit juga dapat digunakan dalam produksi asam nitrat melalui asam sulfat. Reaksi ini pertama kali menghasilkan asam nitrat dan natrium sulfat:
- 2 NaNO2 + H2SO4 → 2 HNO2 + Na2SO4
Asam nitrat kemudian, dalam kondisi normal, terurai:
- 2 HNO2 → NO2 + NO + H2O
Nitrogen dioksida dari dekomposisi sebelumnya kemudian disalurkan melalui kondensor atau peralatan distilasi fraksional untuk bereaksi dengan air dan menghasilkan asam nitrat:
- 2 NO2 + H2O → HNO3 + HNO2
Toksisitas
suntingMeski memiliki kemampuan dalam mencegah pertumbuhan bakteri, senyawa ini dapat menjadi racun dalam jumlah tinggi untuk hewan dan manusia. LD50 natrium nitrit dalam tikus adalah 180 mg/kg dan LDLo pada manusia adalah 71 mg/kg, berarti seorang dengan berat 65 kg harus setidaknya mengkonsumsi 4.6 g untuk mengakibatkan kematian.[9] Untuk mencegah toksisitas tersebut, natrium nitrit (dicampur dengan garam) yang dijual sebagai aditif makanan diwarnai merah muda terang agar tidak terkecoh dengan garam biasa atau gula pasir. Nitrit tidak terdapat secara alami pada sayuran dalam jumlah banyak.[10] Namun, nitrat ditemukan pada sayuran yang tersedia secara komersial. Studi di daerah pertanian intensif di utara Portugal menemukan kadar nitrat residual dalam 34 sampel sayuran, termasuk varietas kubis, selada, bayam, peterseli dan lobak yang berbeda berada pada rentang antara 54 hingga 2440 mg/kg, misalnya kangkung keriting (302.0 mg/kg) dan kembang kol hijau (64 mg/kg).[11][12] Sayuran rebus mengurangi kadar nitrat tetapi tidak bagi nitrit.[11] Daging segar mengandung 0.4–0.5 mg/kg nitrit serta 4–7 mg/kg nitrat (10–30 mg/kg nitrat dalam daging olahan).[10] Kehadiran nitrit dalam jaringan hewan merupakan konsekuensi metabolisme nitrogen monoksida, suatu neurotransmitter penting.[13] Nitrogen monoksida dapat dibuat secara de novo dari nitrit oksida sintase dengan memanfaatan arginin atau dari nitrat atau nitrit yang dikonsumsi tubuh.[14]
Referensi
sunting- ^ T. Gohda, M. Ichikawa (1996). "The Refinement of the Structure of Ferroelectric Sodium Nitrite". Journal of the Korean Physical Society. 29: 551–554.
- ^ Zumdahl, Steven S. (2009). Chemical Principles (Edisi 6th). Houghton Mifflin Company. hlm. A23. ISBN 0-618-94690-X.
- ^ "WHO Model List of EssentialMedicines" (PDF). World Health Organization (dalam bahasa Inggris). April 2015. Diakses tanggal 25 September 2016.
- ^ Wolfgang Laue, Michael Thiemann, Erich Scheibler, Karl Wilhelm Wiegand "Nitrates and Nitrites" dalam Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim.doi:10.1002/14356007.a17_265. Tanggal Posting Artikel Daring: 15 Juni 2000
- ^ Hao, Zhi-wei; Xu, Xin-hua; Wang, Da-hui (Maret 2005). "Reductive denitrification of nitrate by scrap iron filings". Journal of Zhejiang University SCIENCE (dalam bahasa Inggris). 6B (3): 182–186. doi:10.1631/jzus.2005.B0182.
- ^ "Sodium Azide". Hazardous Waste Management (dalam bahasa Inggris). Northeastern University. March 2003. Diarsipkan dari asli tanggal 2007-11-04. Diakses tanggal 2017-07-11.
- ^ Committee on Prudent Practices for Handling, Storage, and Disposal of Chemicals in Laboratories, Board on Chemical Sciences and Technology, Commission on Physical Sciences, Mathematics, and Applications, National Research Council (1995). Prudent practices in the laboratory: handling and disposal of chemicals (dalam bahasa Inggris). Washington, D.C.: National Academy Press. ISBN 0-309-05229-7. Pemeliharaan CS1: Banyak nama: authors list (link)
- ^ Stern, Kurt H. (1972). "High Temperature Properties and Decomposition of Inorganic Salts; Part 3. Nitrates and Nitrites" (PDF). J. Phys. Chem. (dalam bahasa Inggris). 1 (3). US Naval Research Laboratory: 750–751. doi:10.1063/1.3253104. Diarsipkan dari asli (PDF) tanggal 2016-12-21. Diakses tanggal 15 Maret 2014.
- ^ "Salinan arsip". Diarsipkan dari asli tanggal 2008-04-10. Diakses tanggal 2017-07-11.
- ^ a b Dennis, M. J.; Wilson, L. A. (2003). "Nitrates and Nitrites". Encyclopedia of Food Sciences and Nutrition. hlm. 4136. doi:10.1016/B0-12-227055-X/00830-0. ISBN 978-0-12-227055-0.
- ^ a b Leszczyńska, Teresa; Filipiak-Florkiewicz, Agnieszka; Cieślik, Ewa; Sikora, ElżBieta; Pisulewski, Paweł M. (2009). "Effects of some processing methods on nitrate and nitrite changes in cruciferous vegetables". Journal of Food Composition and Analysis. 22 (4): 315–321. doi:10.1016/j.jfca.2008.10.025.
- ^ Correia, Manuela; Barroso, Ângela; Barroso, M. Fátima; Soares, Débora; Oliveira, M. B. P. P.; Delerue-Matos, Cristina (2010). "Contribution of different vegetable types to exogenous nitrate and nitrite exposure". Food Chemistry. 120 (4): 960–966. doi:10.1016/j.foodchem.2009.11.030.
- ^ Meulemans, A.; Delsenne, F. (1994). "Measurement of nitrite and nitrate levels in biological samples by capillary electrophoresis". Journal of Chromatography B. 660 (2): 401–404. doi:10.1016/0378-4347(94)00310-6.
- ^ Southan, G; Srinivasan, A (1998). "Nitrogen Oxides and Hydroxyguanidines: Formation of Donors of Nitric and Nitrous Oxides and Possible Relevance to Nitrous Oxide Formation by Nitric Oxide Synthase". Nitric Oxide. 2 (4): 270–86. doi:10.1006/niox.1998.0187. PMID 9851368.
Pranala luar
sunting- (Inggris) ATSDR – Case Studies in Environmental Medicine – Nitrate/Nitrite Toxicity U.S. Department of Health and Human Services (domain umum)
- (Inggris) International Chemical Safety Card 1120.
- (Inggris) National Center for Home Food Preservation Nitrates and Nitrites Diarsipkan 2005-04-02 di Wayback Machine..
- (Inggris) TR-495: Toxicology and Carcinogenesis Studies of Sodium Nitrite (CAS NO. 7632-00-0) Drinking Water Studies in F344/N Rats and B6C3F1 Mice.
- (Inggris) Nitrit dalam Daging Diarsipkan 2011-01-01 di Wayback Machine.

