
| |

| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Sulfurous diklorida
| |
Nama lain
| |
| Penanda | |
Model 3D (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
| Nomor UN | 1836 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| SOCl2 | |
| Massa molar | 118.97 g/mol |
| Penampilan | cairan bening, tak berwarna (kuning akibat penuaan) |
| Bau | menyengat dan tidak menyenangkan |
| Densitas | 1.638 g/cm3, cairan |
| Titik lebur | −1.045 °C (−1.849 °F; −772 K) |
| Titik didih | 746 °C (1.375 °F; 1.019 K) |
| bereaksi | |
| Kelarutan | Larut dalam kebanyakan pelarut aprotik: toluena, kloroform, dietil eter. Bereaksi dengan pelarut protik: MeOH dll |
| Tekanan uap |
|
| Indeks bias (nD) | 1.517 (20 °C)[2] |
| Viskositas | 0.6 cP |
| Struktur | |
| piramidal | |
| 1.44 D | |
| Termokimia | |
| Kapasitas kalor (C) | 121.0 kJ/mol (cair)[3] |
| Entropi molar standar (S |
309.8 kJ/mol (gas)[3] |
| Entalpi pembentukan standar (ΔfH |
-245.6 kJ/mol (cair)[3] |
| Bahaya | |
| Bahaya utama |
|
| Piktogram GHS |   
|
| Keterangan bahaya GHS | {{{value}}} |
| H302, H314, H331 | |
| P261, P280, P305+P351+P338, P310 | |
| Titik nyala | Tidak mudah terbakar[4] |
| Batas imbas kesehatan AS (NIOSH): | |
PEL (yang diperbolehkan)
|
none[4] |
REL (yang direkomendasikan)
|
C 1 ppm (5 mg/m3)[4] |
IDLH (langsung berbahaya)
|
N.D.[4] |
| Senyawa terkait | |
Related tionil halida
|
|
Senyawa terkait
|
|
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Tionil klorida adalah suatu senyawa anorganik dengan rumus kimia SOCl2. Cairan ini sangat mudah menguap dan berbau tidak sedap. Tionil klorida terutama digunakan sebagai pereaksi klorinasi, dengan sekitar 45,000 ton per tahun diproduksi pada awal tahun 1990an.[5] Senyawa ini beracun dan akan bereaksi keras dengan air untuk menghasilkan gas beracun, juga terdaftar sebagai senyawa Schedule 3 karena dapat digunakan untuk produksi senjata kimia.
Banyak yang tidak dapat membedakan antara tionil klorida dengan sulfuril klorida, SO2Cl2, namun sifat senyawa ini berbeda secara signifikan. Sulfuril klorida adalah sumber klor sedangkan tionil klorida merupakan sumber ion klorida.
Produksi
suntingSintesis utama senyawa ini dalam industri melibatkan reaksi belerang trioksida dan belerang diklorida:[6]
- SO3 + SCl2 → SOCl2 + SO2
Metode lainnya termasuk sintesis dari fosfor pentaklorida, klorin dan belerang diklorida, atau fosgen:
- SO2 + PCl5 → SOCl2 + POCl3
- SO2 + Cl2 + SCl2 → 2 SOCl2
- SO3 + Cl2 + 2 SCl2 → 3 SOCl2
- SO2 + COCl2 → SOCl2 + CO2
Yang pertama dari empat reaksi di atas juga memberi fosfor oksiklorida (fosforil klorida), yang menyerupai tionil klorida dalam banyak reaksinya.
Sifat dan struktur
sunting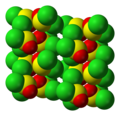
SOCl2 mengadopsi geometri molekul piramidal dengan simetri molekul Cs Geometri ini dikaitkan dengan efek dari pasangan elektron sunyi di pusat belerang(IV).
Dalam keadaan padat SOCl2 membentuk kristal monoklinik dengan grup ruang P21/c.[7]
Kestabilan
suntingTionil klorida Memiliki umur simpan yang panjang, namun sampel "tua" mengembangkan rona berwarna kuning, mungkin karena pembentukan disulfur diklorida. Senyawa ini perlahan terdekomposisi menjadi S2Cl2, SO2 dan Cl2 pada sedikit di atas titik didih.[6][8] Tionil klorida rentan terhadap fotolisis, yang terutama berlanjut melalui mekanisme radikal.[9] Sampel yang menunjukkan tanda-tanda penuaan dapat dimurnikan dengan distilasi di bawah tekanan rendah, untuk memberi cairan yang tidak berwarna.[10]
Reaksi
suntingTionil klorida terutama digunakan dalam produksi industri senyawa organoklorin, yang sering kali merupakan zat antara obat-obatan dan agrikultur. Biasanya lebih disukai daripada pereaksi lainnya, seperti fosfor pentaklorida, sebagai produk sampingannya (HCl dan SO2) adalah gas, yang menyederhanakan pemurnian produk.
Banyak produk tionil klorida sendiri sangat reaktif dan karena itu melibatkan berbagai reaksi.
Dengan spesi oksigen
suntingTionil klorida bereaksi dengan air untuk membentuk sulfur dioksida dan asam klorida. Proses ini sangat eksotermik.
- SOCl2 + H2O → 2 HCl + SO2
Secara klasik, ia mengubah asam karboksilat menjadi asil klorida.[11][12][13]
- SOCl2 + RCO2H → RC(O)Cl + SO2 + HCl
Dengan proses yang sama, juga mengubah alkohol menjadi alkil klorida. Jika alkoholnya kiral, reaksi tersebut umumnya berlanjut melalui mekanisme SNi dengan mempertahankan stereokimia;[14] tetapi, tergantung pada kondisi pasti yang digunakan, stereo-inversi juga dapat dicapai. Secara historis penggunaan SOCl2 dalam kombinasi dengan amina tersier seperti piridin disebut halogenasi Darzens namun nama ini jarang digunakan oleh ahli kimia modern.

Reaksi dengan kelebihan alkohol menghasilkan ester sulfit, yang dapat menjadi pereaksi metilasi, alkilasi dan hidroksialkilasi yang kuat.[15]
- SOCl2 + 2 ROH → (RO)2SO + 2 HCl
Contohnya, penambahan SOCl2 pada asam amino dalam metanol secara selektif menghasilkan metil ester yang sesuai.[16]
Dengan spesi nitrogen
suntingDengan amina primer, thionil klorida memberikan turunan sulfinamina (RNSO), satu contohnya adalah N-sulfinilanilin. Tionil klorida bereaksi dengan senyawa utama formamida untuk membentuk isosianida[17] dan dengan formamida sekunder untuk menghasilkan ion kloroiminium; Seperti reaksi dengan dimetilformamida akan membentuk pereaksi Vilsmeier.[18] Dengan proses analog primer amida akan bereaksi dengan tionil klorida untuk membentuk imidoil klorida, dengan amida sekunder juga memberi ion kloroiminium. Spesi ini sangat reaktif dan dapat digunakan untuk mengkatalisis konversi asam karboksilat menjadi asil klorida, mereka juga dieksploitasi dalam reaksi Bischler–Napieralski sebagai alat untuk membentuk isokuinolin.

Amida primer akan terus terbentuk nitril jika dipanaskan (degradasi amida Von Braun).[19] Tionil klorida juga telah digunakan untuk mempromosikan penataan ulang Beckmann dari oksima.
Keamanan
suntingSOCl2 aalah senyawa reaktif yang dapat dengan keras dan/atau secara eksplosif melepaskan gas berbahaya pada kontak dengan air dan pereaksi lainnya. Tionil klorida dikontrol di bawah Konvensi Senjata Kimia, di mana tercantum di dalamnya Schedule 3. Tionil klorida digunakan dalam metode "di-di" untuk memproduksi agen saraf seri-G.
Lihat pula
suntingReferensi
sunting- ^ Thionyl chloride dalam Linstrom, P.J.; Mallard, W.G. (eds.) NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD. http://webbook.nist.gov (diakses tanggal 2014-05-11)
- ^ Patnaik, Pradyot (2003). Handbook of inorganic chemicals. New York, NY [u.a.]: McGraw-Hill. ISBN 0-07-049439-8.
- ^ a b c Lide, ed.-in-chief David R. (1996). CRC handbook of chemistry and physics (Edisi 76.). Boca Raton, Fla.: CRC Press. hlm. 5–10. ISBN 0-8493-0476-8.
- ^ a b c d "NIOSH Pocket Guide to Chemical Hazards #0611". National Institute for Occupational Safety and Health (NIOSH).
- ^ Hans-Dietrich Lauss, Wilfried Steffens “Sulfur Halides” in Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, Weinheim, 2005.doi:10.1002/14356007.a25_623
- ^ a b Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (Edisi 2), Oxford: Butterworth-Heinemann, hlm. 694, ISBN 0-7506-3365-4 Pemeliharaan CS1: Banyak nama: authors list (link)
- ^ Mootz, D.; Merschenz-Quack, A. (15 May 1988). "Structures of thionyl halides: SOCl2 dan SOBr2". Acta Crystallographica Section C. 44 (5): 926–927. doi:10.1107/S010827018800085X.
- ^ Riley, edited by Georg Brauer ; translated by Scripta Technica, Inc. Translation editor Reed F. (1963). Handbook of preparative inorganic chemistry. Volume 1 (Edisi 2nd). New York, N.Y.: Academic Press. hlm. 383. ISBN 978-0121266011. ; Pemeliharaan CS1: Banyak nama: authors list (link)
- ^ Donovan, R. J.; Husain, D.; Jackson, P. T. (1969). "Spectroscopic and kinetic studies of the SO radical and the photolysis of thionyl chloride". Transactions of the Faraday Society. 65: 2930. doi:10.1039/TF9696502930.
- ^ Friedman, Lester; Wetter, William P. (1967). "Purification of thionyl chloride". Journal of the Chemical Society A: Inorganic, Physical, Theoretical: 36. doi:10.1039/J19670000036.
- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (Edisi 1st). Oxford University Press. hlm. 295. ISBN 978-0-19-850346-0.
- ^ Allen, C. F. H.; Byers, Jr., J. R.; Humphlett, W. J. (1963). "Oleoyl chloride". Org. Synth.; Coll. Vol. 4: 739.
- ^ Rutenberg, M. W.; Horning, E. C. (1963). "1-Methyl-3-ethyloxindole". Org. Synth.; Coll. Vol. 4: 620.
- ^ Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (Edisi 6), New York: Wiley-Interscience, hlm. 469, ISBN 0-471-72091-7 Pemeliharaan CS1: Banyak nama: authors list (link)
- ^ van Woerden, H. F. (1963). "Organic Sulfites". Chemical Reviews. 63 (6): 557–571. doi:10.1021/cr60226a001.
- ^ Brenner, M.; Huber, W. (1953). "Herstellung von α-Aminosäureestern durch Alkoholyse der Methylester". Helvetica Chimica Acta (dalam bahasa German). 36 (5): 1109–1115. doi:10.1002/hlca.19530360522. Pemeliharaan CS1: Bahasa yang tidak diketahui (link)
- ^ Niznik, G. E.; Morrison, III, W. H.; Walborsky, H. M. (1988). "1-d-Aldehydes from organometallic reagents: 2-methylbutanal-1-d". Org. Synth.; Coll. Vol. 6: 751.
- ^ Arrieta, A; Aizpurua, J.M; Palomo, C (1984). "N,N-Dimethylchlorosulfitemethaniminium chloride (SOCl2-DMF) a versatile dehydrating reagent". Tetrahedron Letters. 25 (31): 3365–3368. doi:10.1016/S0040-4039(01)81386-1.
- ^ Krynitsky, J. A.; Carhart, H. W. (1963). "2-Ethylhexanonitrile". Org. Synth.; Coll. Vol. 4: 436.